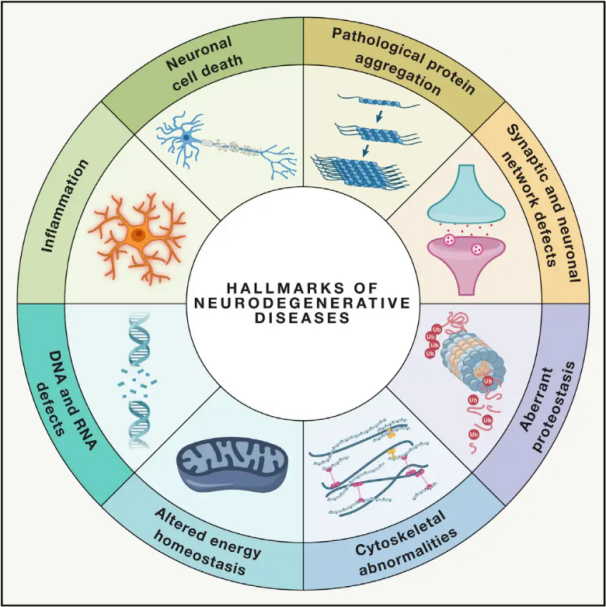
ជំងឺសរសៃប្រសាទដែលខូចទ្រង់ទ្រាយ(NDDs) ត្រូវបានកំណត់លក្ខណៈដោយការបាត់បង់ជាលំដាប់ ឬជាប់លាប់នៃចំនួនប្រជាជនណឺរ៉ូនដែលងាយរងគ្រោះជាក់លាក់នៅក្នុងខួរក្បាល ឬខួរឆ្អឹងខ្នង។ ការចាត់ថ្នាក់នៃ NDDs អាចផ្អែកលើលក្ខណៈវិនិច្ឆ័យផ្សេងៗ រួមទាំងការចែកចាយកាយវិភាគសាស្ត្រនៃការខូចសរសៃប្រសាទ (ដូចជាជំងឺ extrapyramidal ការខូចសរសៃប្រសាទ frontotemporal ឬ spinocerebellar ataxias) ភាពមិនប្រក្រតីនៃម៉ូលេគុលបឋម (ដូចជា amyloid-β, prions, tau ឬ α-synuclein) ឬលក្ខណៈពិសេសគ្លីនិកសំខាន់ៗ (ដូចជាជំងឺ Parkinson, amyotrophic lateral sclerosis និង dementia)។ ទោះបីជាមានភាពខុសគ្នាទាំងនេះនៅក្នុងចំណាត់ថ្នាក់ និងការបង្ហាញរោគសញ្ញាក៏ដោយ ជំងឺដូចជាជំងឺ Parkinson (PD), Amyotrophic Lateral Sclerosis (ALS) និងជំងឺ Alzheimer (AD) មានដំណើរការមូលដ្ឋានទូទៅដែលនាំទៅដល់មុខងារមិនប្រក្រតីនៃណឺរ៉ូន និងការស្លាប់កោសិកានៅទីបំផុត។
ដោយសារមនុស្សរាប់លាននាក់នៅទូទាំងពិភពលោករងផលប៉ះពាល់ដោយជំងឺ NDDs អង្គការសុខភាពពិភពលោកប៉ាន់ប្រមាណថា នៅឆ្នាំ 2040 ជំងឺទាំងនេះនឹងក្លាយជាមូលហេតុចម្បងទីពីរនៃការស្លាប់នៅក្នុងប្រទេសអភិវឌ្ឍន៍។ ខណៈពេលដែលមានការព្យាបាលជាច្រើនដែលអាចរកបានដើម្បីបំបាត់ និងគ្រប់គ្រងរោគសញ្ញាដែលទាក់ទងនឹងជំងឺជាក់លាក់ វិធីសាស្ត្រមានប្រសិទ្ធភាពក្នុងការបន្ថយ ឬព្យាបាលការវិវត្តនៃស្ថានភាពទាំងនេះនៅតែពិបាកយល់។ ការសិក្សាថ្មីៗបង្ហាញពីការផ្លាស់ប្តូរគំរូនៃការព្យាបាលពីការគ្រប់គ្រងរោគសញ្ញាសាមញ្ញទៅជាការប្រើប្រាស់យន្តការការពារកោសិកាដើម្បីការពារការខ្សោះជីវជាតិបន្ថែមទៀត។ ភស្តុតាងយ៉ាងទូលំទូលាយបង្ហាញថា ភាពតានតឹងអុកស៊ីតកម្ម និងការរលាកដើរតួនាទីយ៉ាងសំខាន់ក្នុងការបំផ្លាញសរសៃប្រសាទ ដោយដាក់យន្តការទាំងនេះជាគោលដៅសំខាន់សម្រាប់ការការពារកោសិកា។ ក្នុងប៉ុន្មានឆ្នាំថ្មីៗនេះ ការស្រាវជ្រាវជាមូលដ្ឋាន និងគ្លីនិកបានបង្ហាញពីសក្តានុពលនៃការព្យាបាលដោយអុកស៊ីសែនសម្ពាធខ្ពស់ (HBOT) ក្នុងការព្យាបាលជំងឺដែលបំផ្លាញសរសៃប្រសាទ។
ការយល់ដឹងអំពីការព្យាបាលដោយអុកស៊ីសែនសម្ពាធខ្ពស់ (HBOT)
ការព្យាបាលដោយប្រើ HBOT ជាធម្មតាពាក់ព័ន្ធនឹងការបង្កើនសម្ពាធដល់បរិយាកាសដាច់ខាតលើសពី 1 (ATA) — សម្ពាធនៅកម្រិតទឹកសមុទ្រ — សម្រាប់រយៈពេល 90-120 នាទី ដែលជារឿយៗតម្រូវឱ្យមានវគ្គច្រើនដងអាស្រ័យលើស្ថានភាពជាក់លាក់ដែលកំពុងត្រូវបានព្យាបាល។ សម្ពាធខ្យល់ដែលប្រសើរឡើងធ្វើអោយប្រសើរឡើងនូវការដឹកជញ្ជូនអុកស៊ីសែនទៅកាន់កោសិកា ដែលវាជំរុញដល់ការរីកសាយនៃកោសិកាដើម និងបង្កើនដំណើរការព្យាបាលដែលសម្របសម្រួលដោយកត្តាលូតលាស់មួយចំនួន។
ដើមឡើយ ការអនុវត្ត HBOT ត្រូវបានបង្កើតឡើងដោយផ្អែកលើច្បាប់ Boyle-Marriott ដែលបង្ហាញពីការកាត់បន្ថយពពុះឧស្ម័នដែលពឹងផ្អែកលើសម្ពាធ រួមជាមួយនឹងអត្ថប្រយោជន៍នៃកម្រិតអុកស៊ីសែនខ្ពស់នៅក្នុងជាលិកា។ មានរោគសាស្ត្រជាច្រើនដែលគេដឹងថាទទួលបានអត្ថប្រយោជន៍ពីស្ថានភាពអុកស៊ីហ្សែនខ្ពស់ដែលផលិតដោយ HBOT រួមទាំងជាលិកាងាប់ របួសដោយវិទ្យុសកម្ម របួស រលាក រោគសញ្ញាបន្ទប់ និងដំបៅរលួយឧស្ម័ន ក្នុងចំណោមរោគសាស្ត្រផ្សេងទៀតដែលបានចុះបញ្ជីដោយសមាគមវេជ្ជសាស្ត្រក្រោមសមុទ្រ និង Hyperbaric។ ជាពិសេស HBOT ក៏បានបង្ហាញពីប្រសិទ្ធភាពជាការព្យាបាលបន្ថែមនៅក្នុងគំរូជំងឺរលាក ឬជំងឺឆ្លងផ្សេងៗ ដូចជាជំងឺរលាកពោះវៀនធំ និងការឆ្លងមេរោគក្នុងឈាម។ ដោយសារតែយន្តការប្រឆាំងនឹងការរលាក និងអុកស៊ីតកម្មរបស់វា HBOT ផ្តល់នូវសក្តានុពលយ៉ាងសំខាន់ជាមធ្យោបាយព្យាបាលសម្រាប់ជំងឺសរសៃប្រសាទ។
ការសិក្សាមុនព្យាបាលនៃការព្យាបាលដោយអុកស៊ីសែនសម្ពាធខ្ពស់ក្នុងជំងឺសរសៃប្រសាទដែលខូចទ្រង់ទ្រាយ៖ ការយល់ដឹងពីគំរូកណ្ដុរ 3×Tg
ការសិក្សាមួយក្នុងចំណោមការសិក្សាគួរឱ្យកត់សម្គាល់ផ្តោតលើគំរូកណ្ដុរ 3×Tg នៃជំងឺភ្លេចភ្លាំង (AD) ដែលបានបង្ហាញពីសក្តានុពលព្យាបាលរបស់ HBOT ក្នុងការកែលម្អឱនភាពនៃការយល់ដឹង។ ការស្រាវជ្រាវនេះពាក់ព័ន្ធនឹងកណ្ដុរឈ្មោល 3×Tg អាយុ 17 ខែ បើប្រៀបធៀបទៅនឹងកណ្ដុរឈ្មោល C57BL/6 អាយុ 14 ខែ ដែលបម្រើជាក្រុមត្រួតពិនិត្យ។ ការសិក្សាបានបង្ហាញថា HBOT មិនត្រឹមតែធ្វើអោយប្រសើរឡើងនូវមុខងារនៃការយល់ដឹងប៉ុណ្ណោះទេ ប៉ុន្តែថែមទាំងកាត់បន្ថយការរលាក បន្ទុកបន្ទះ និងការបង្កើតផូស្វ័រ Tau យ៉ាងច្រើនផងដែរ ដែលជាដំណើរការសំខាន់មួយដែលទាក់ទងនឹងរោគសាស្ត្រ AD។
ផលប៉ះពាល់ការពាររបស់ HBOT ត្រូវបានសន្មតថាជាការថយចុះនៃការរលាកសរសៃប្រសាទ។ នេះត្រូវបានបង្ហាញដោយការថយចុះនៃការរីកសាយនៃមីក្រូគ្លីយ៉ាល អាស្ត្រូគ្លីស៊ីស និងការបញ្ចេញស៊ីតូគីនបង្ករលាក។ ការរកឃើញទាំងនេះសង្កត់ធ្ងន់លើតួនាទីពីររបស់ HBOT ក្នុងការបង្កើនប្រសិទ្ធភាពនៃការយល់ដឹង ខណៈពេលដែលក្នុងពេលដំណាលគ្នាកាត់បន្ថយដំណើរការរលាកសរសៃប្រសាទដែលទាក់ទងនឹងជំងឺអាល់ហ្សៃមឺរ។
គំរូមុនព្យាបាលមួយផ្សេងទៀតបានប្រើប្រាស់កណ្ដុរ 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP) ដើម្បីវាយតម្លៃយន្តការការពាររបស់ HBOT លើមុខងារណឺរ៉ូន និងសមត្ថភាពម៉ូទ័រ។ លទ្ធផលបានបង្ហាញថា HBOT បានរួមចំណែកដល់សកម្មភាពម៉ូទ័រ និងកម្លាំងក្តាប់ប្រសើរឡើងនៅក្នុងកណ្ដុរទាំងនេះ ដែលជាប់ទាក់ទងនឹងការកើនឡើងនៃការបញ្ជូនសញ្ញាជីវសាស្ត្រមីតូខនឌ្រី ជាពិសេសតាមរយៈការធ្វើឱ្យសកម្មនៃ SIRT-1, PGC-1α និង TFAM។ នេះបង្ហាញពីតួនាទីសំខាន់នៃមុខងារមីតូខនឌ្រីនៅក្នុងឥទ្ធិពលការពារសរសៃប្រសាទរបស់ HBOT។
យន្តការនៃ HBOT ក្នុងជំងឺសរសៃប្រសាទ
គោលការណ៍ជាមូលដ្ឋាននៃការប្រើប្រាស់ HBOT សម្រាប់ជំងឺសរសៃប្រសាទមិនប្រក្រតី (NDDs) ស្ថិតនៅក្នុងទំនាក់ទំនងរវាងការផ្គត់ផ្គង់អុកស៊ីសែនដែលថយចុះ និងភាពងាយនឹងទទួលរងនូវការផ្លាស់ប្តូរសរសៃប្រសាទ។ កត្តាបង្កឡើងដោយកង្វះអុកស៊ីសែន-1 (HIF-1) ដើរតួនាទីយ៉ាងសំខាន់ជាកត្តាចម្លងដែលអនុញ្ញាតឱ្យកោសិកាសម្របខ្លួនទៅនឹងភាពតានតឹងអុកស៊ីសែនទាប ហើយត្រូវបានចោទប្រកាន់នៅក្នុងជំងឺសរសៃប្រសាទមិនប្រក្រតីជាច្រើនរួមទាំង AD, PD, ជំងឺ Huntington និង ALS ដែលសម្គាល់វាថាជាគោលដៅថ្នាំដ៏សំខាន់។
ដោយសារតែអាយុជាកត្តាហានិភ័យដ៏សំខាន់សម្រាប់ជំងឺសរសៃប្រសាទច្រើនប្រភេទ ការស៊ើបអង្កេតផលប៉ះពាល់នៃ HBOT លើជីវវិទ្យាសរសៃប្រសាទចាស់ជរាគឺមានសារៈសំខាន់។ ការសិក្សាបានបង្ហាញថា HBOT អាចធ្វើអោយប្រសើរឡើងនូវឱនភាពនៃការយល់ដឹងទាក់ទងនឹងអាយុចំពោះមនុស្សចាស់ដែលមានសុខភាពល្អ។លើសពីនេះ អ្នកជំងឺវ័យចំណាស់ដែលមានការចុះខ្សោយនៃការចងចាំយ៉ាងធ្ងន់ធ្ងរបានបង្ហាញពីភាពប្រសើរឡើងនៃការយល់ដឹង និងការកើនឡើងនៃលំហូរឈាមខួរក្បាលបន្ទាប់ពីការប៉ះពាល់នឹង HBOT។
១. ផលប៉ះពាល់នៃ HBOT លើការរលាក និងភាពតានតឹងអុកស៊ីតកម្ម
HBOT បានបង្ហាញពីសមត្ថភាពក្នុងការកាត់បន្ថយការរលាកសរសៃប្រសាទចំពោះអ្នកជំងឺដែលមានមុខងារខួរក្បាលមិនប្រក្រតីធ្ងន់ធ្ងរ។ វាមានសមត្ថភាពបន្ថយកម្រិត cytokines ដែលបង្កការរលាក (ដូចជា IL-1β, IL-12, TNFα និង IFNγ) ខណៈពេលដែលបង្កើនកម្រិត cytokines ប្រឆាំងនឹងការរលាក (ដូចជា IL-10)។ អ្នកស្រាវជ្រាវមួយចំនួនបានស្នើថា ប្រភេទអុកស៊ីសែនដែលមានប្រតិកម្ម (ROS) ដែលបង្កើតឡើងដោយ HBOT សម្របសម្រួលផលប៉ះពាល់ជាច្រើននៃការព្យាបាល។ ជាលទ្ធផល ក្រៅពីសកម្មភាពកាត់បន្ថយពពុះដែលពឹងផ្អែកលើសម្ពាធ និងការសម្រេចបាននូវកម្រិតអុកស៊ីសែនជាលិកាខ្ពស់ លទ្ធផលវិជ្ជមានដែលភ្ជាប់ទៅនឹង HBOT គឺអាស្រ័យមួយផ្នែកលើតួនាទីសរីរវិទ្យានៃ ROS ដែលផលិត។
2. ផលប៉ះពាល់នៃ HBOT លើ Apoptosis និងការការពារសរសៃប្រសាទ
ការស្រាវជ្រាវបានបង្ហាញថា HBOT អាចកាត់បន្ថយការ phosphorylation hippocampus នៃ p38 mitogen-activated protein kinase (MAPK) ដែលក្រោយមកធ្វើអោយប្រសើរឡើងនូវការយល់ដឹង និងកាត់បន្ថយការខូចខាត hippocampus។ ទាំង HBOT ដែលឈរតែឯង និងរួមផ្សំជាមួយនឹងសារធាតុចម្រាញ់ Ginkgo biloba ត្រូវបានគេរកឃើញថាបន្ថយការបញ្ចេញមតិរបស់ Bax និងសកម្មភាពរបស់ caspase-9/3 ដែលបណ្តាលឱ្យអត្រា apoptosis ថយចុះនៅក្នុងគំរូសត្វកកេរដែលបង្កឡើងដោយ aβ25-35។ លើសពីនេះ ការសិក្សាមួយផ្សេងទៀតបានបង្ហាញថា ការកំណត់លក្ខខណ្ឌជាមុនរបស់ HBOT បានបង្កឱ្យមានការអត់ធ្មត់ប្រឆាំងនឹងការខ្វះឈាមខួរក្បាល ជាមួយនឹងយន្តការដែលពាក់ព័ន្ធនឹងការកើនឡើងនៃការបញ្ចេញមតិ SIRT1 រួមជាមួយនឹងកម្រិត augmented B-cell lymphoma 2 (Bcl-2) និងការថយចុះ caspase-3 សកម្ម ដែលបញ្ជាក់ពីលក្ខណៈសម្បត្តិការពារសរសៃប្រសាទ និងប្រឆាំងនឹង apoptosis របស់ HBOT។
៣. ឥទ្ធិពលរបស់ HBOT លើចរន្តឈាម និងការបង្កើតសរសៃប្រសាទ
ការប៉ះពាល់នឹង HBOT ត្រូវបានផ្សារភ្ជាប់ជាមួយនឹងផលប៉ះពាល់ច្រើនទៅលើប្រព័ន្ធសរសៃឈាមខួរក្បាល រួមទាំងការបង្កើនភាពជ្រាបចូលនៃរបាំងឈាម-ខួរក្បាល ការជំរុញ angiogenesis និងការកាត់បន្ថយការហើម។ បន្ថែមពីលើការផ្តល់ការផ្គត់ផ្គង់អុកស៊ីសែនកាន់តែច្រើនដល់ជាលិកា HBOT...ជំរុញការបង្កើតសរសៃឈាមតាមរយៈការធ្វើឱ្យសកម្មនូវកត្តាប្រតិចារិកដូចជាកត្តាលូតលាស់នៃស្រទាប់ខាងក្នុងសរសៃឈាម និងដោយការជំរុញការរីកសាយនៃកោសិកាដើមសរសៃប្រសាទ។
៤. ផលប៉ះពាល់អេពីហ្សែនទិចនៃ HBOT
ការសិក្សាបានបង្ហាញថា ការប៉ះពាល់នឹងអុកស៊ីសែន hyperbaric នៃកោសិកា endothelial មីក្រូសរសៃឈាមរបស់មនុស្ស (HMEC-1) គ្រប់គ្រងហ្សែនចំនួន 8,101 យ៉ាងសំខាន់ រួមទាំងការបញ្ចេញមតិដែលកើនឡើង និងថយចុះ ដែលបង្ហាញពីការកើនឡើងនៃការបញ្ចេញមតិហ្សែនដែលទាក់ទងនឹងផ្លូវឆ្លើយតបប្រឆាំងអុកស៊ីតកម្ម។
សេចក្តីសន្និដ្ឋាន
ការប្រើប្រាស់ HBOT បានឈានទៅមុខគួរឱ្យកត់សម្គាល់តាមពេលវេលា ដោយបង្ហាញពីភាពអាចរកបាន ភាពជឿជាក់ និងសុវត្ថិភាពរបស់វានៅក្នុងការអនុវត្តគ្លីនិក។ ខណៈពេលដែល HBOT ត្រូវបានរុករកជាការព្យាបាលក្រៅស្លាកសញ្ញាសម្រាប់ NDDs ហើយការស្រាវជ្រាវមួយចំនួនត្រូវបានធ្វើឡើង នៅតែមានតម្រូវការបន្ទាន់សម្រាប់ការសិក្សាយ៉ាងម៉ត់ចត់ដើម្បីធ្វើឱ្យការអនុវត្ត HBOT មានស្តង់ដារក្នុងការព្យាបាលលក្ខខណ្ឌទាំងនេះ។ ការស្រាវជ្រាវបន្ថែមគឺចាំបាច់ដើម្បីកំណត់ភាពញឹកញាប់នៃការព្យាបាលដ៏ល្អប្រសើរ និងវាយតម្លៃវិសាលភាពនៃផលប៉ះពាល់ដែលមានប្រយោជន៍សម្រាប់អ្នកជំងឺ។
សរុបមក ចំនុចប្រសព្វនៃអុកស៊ីសែនសម្ពាធខ្ពស់ និងជំងឺសរសៃប្រសាទដែលខូចទ្រង់ទ្រាយ បង្ហាញពីព្រំដែនដ៏ជោគជ័យមួយក្នុងលទ្ធភាពព្យាបាល ដែលទាមទារឱ្យមានការរុករក និងការផ្ទៀងផ្ទាត់ជាបន្តបន្ទាប់នៅក្នុងការកំណត់គ្លីនិក។
ពេលវេលាបង្ហោះ៖ ថ្ងៃទី ១៦ ខែឧសភា ឆ្នាំ ២០២៥

